在化学学习中,电子式是一种非常重要的表示方法,它用于直观地展示原子或分子中电子的排布情况。对于初学者来说,掌握电子式的书写方法显得尤为重要。本文将从基础概念入手,详细介绍电子式的书写步骤和注意事项,并辅以实例,帮助读者全面了解如何书写电子式。
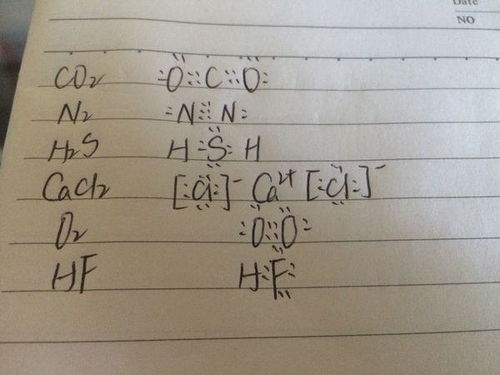
一、电子式的基本概念
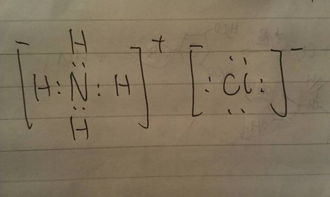
电子式是一种用小黑点“.”或叉号“×”来表示原子最外层电子排布的式子。小黑点或叉号均表示电子,它们所处的位置表示电子在核外的空间分布,而小黑点的数目则表示该元素的原子在形成化学键时表现出来的化合价。电子式主要用于描述共价化合物、离子化合物以及单质分子的电子排布情况。
二、电子式的书写规则
1. 原子的电子式
对于原子来说,其电子式就是在元素符号的周围用小黑点或叉号来表示其最外层的电子数。例如,氢原子的电子式为H·(或H×),表示氢原子最外层有一个电子;氧原子的电子式为O∶∶(或O××),表示氧原子最外层有六个电子。
2. 离子的电子式
离子是由原子得失电子后形成的带电粒子。在书写离子的电子式时,我们需要根据离子所带的电荷数,在原子电子式的基础上进行相应的调整。对于阳离子来说,其电子式就是原子电子式失去相应的电子后形成的;对于阴离子来说,其电子式则是在原子电子式的基础上增加相应的电子数。例如,钠离子(Na⁺)的电子式为Na⁺(在Na的右上角标出“+”号,表示失去一个电子);氯离子(Cl⁻)的电子式为∶Cl∶(在Cl的周围增加两个电子,同时在其右上角标出“-”号,表示得到一个电子)。
3. 共价化合物的电子式
共价化合物是由非金属元素之间通过共用电子对形成的化合物。在书写共价化合物的电子式时,我们需要按照各原子的最外层电子数,将原子进行排列,并用小黑点或叉号表示出它们之间的共用电子对。例如,水分子(H₂O)的电子式为H∶O∶H(两个氢原子和一个氧原子之间通过两对共用电子对相连)。
4. 离子化合物的电子式
离子化合物是由阳离子和阴离子通过离子键结合而成的化合物。在书写离子化合物的电子式时,我们需要分别写出阳离子和阴离子的电子式,然后将它们结合在一起。注意,在离子化合物中,阴离子需要带有方括号,并在方括号的右上角标出其所带的电荷数(负号)。例如,氯化钠(NaCl)的电子式为Na⁺[∶Cl∶]⁻(钠离子和氯离子之间通过离子键相连,氯离子带有方括号和负号)。
三、电子式的书写步骤
1. 确定化合物的类型
在书写电子式之前,我们首先需要确定化合物的类型,是共价化合物还是离子化合物。这可以通过化合物的组成元素来判断。一般来说,由非金属元素组成的化合物是共价化合物;由金属元素和非金属元素组成的化合物是离子化合物。
2. 写出各原子的电子式
根据化合物的类型,我们分别写出各原子的电子式。对于共价化合物来说,我们需要写出所有参与成键的原子的电子式;对于离子化合物来说,我们需要分别写出阳离子和阴离子的电子式。
3. 排列原子并连接电子
对于共价化合物来说,我们按照各原子的最外层电子数和化合价,将原子进行排列,并用小黑点或叉号表示出它们之间的共用电子对。对于离子化合物来说,我们将阳离子和阴离子按照离子键的方式结合在一起,并在阴离子周围加上方括号和负号。
4. 检查并修正
在完成电子式的书写后,我们需要对其进行检查,确保所有原子的最外层电子数都达到了稳定结构(即8电子稳定结构,对于氢原子和氦原子等少数元素来说,2电子稳定结构也是可能的)。如果发现有不符合稳定结构的情况,我们需要对电子式进行修正。
四、电子式书写的注意事项
1. 注意原子序数和化合价的关系
在书写电子式时,我们需要注意原子序数和化合价的关系。原子序数决定了原子的电子排布情况,而化合价则决定了原子在形成化学键时表现出来的电子数。因此,在书写电子式时,我们需要根据原子的化合价来确定其最外层的电子数。
2. 注意共用电子对的表示方法
在书写共价化合物的电子式时,我们需要注意共用电子对的表示方法。共用电子对是由两个原子共同使用的电子对,它们将两个原子连接在一起形成化学键。在表示共用电子对时,我们通常使用一对小黑点或叉号来表示。
3. 注意离子
































相关文章